Developmental Cell :刘光慧团队建立血管和神经类器官模型,揭示人类衰老与疾病机制
来源:生物世界 2025-11-30 10:46
该研究利用基因编辑和人多能干细胞定向分化技术,首次成功构建了模拟 HGPS 的人类血管类器官模型。
类器官模型作为生命科学研究的前沿工具,为模拟人类器官发育、衰老和疾病过程提供了强大平台。近日,中国科学院动物研究所刘光慧研究员团队与合作者通过构建血管和神经类器官模型,分别揭示了器官稳态建立和衰老的关键机制。这些成果不仅深化了对人类发育和衰老规律的理解,也为相关疾病的干预提供了新靶点。
血管类器官模型揭示 SRF 下调驱动人类血管衰老
血管衰老是心血管疾病的主要驱动因素,而心血管疾病是全球老年人口死亡的首要原因。哈钦森-吉尔福德早衰综合征(HGPS)是一种由 LMNA 基因突变引起的罕见儿童早衰性疾病,患者表现出加速的全身性衰老,其中进行性血管病变尤为突出,常因心脑血管并发症早夭,平均寿命仅约 14.5 岁。由于缺乏能够复现人类血管复杂三维结构及体内病理特征的模型,深入研究血管衰老机制一直面临挑战。
近日,刘光慧研究员与中国科学院北京基因组研究所张维绮研究员合作,在 Cell 子刊 Developmental Cell 发表了题为:Vascular organoid model of Hutchinson-Gilford progeria syndrome uncovers repression of the SRF pathway in premature aging 的研究论文。

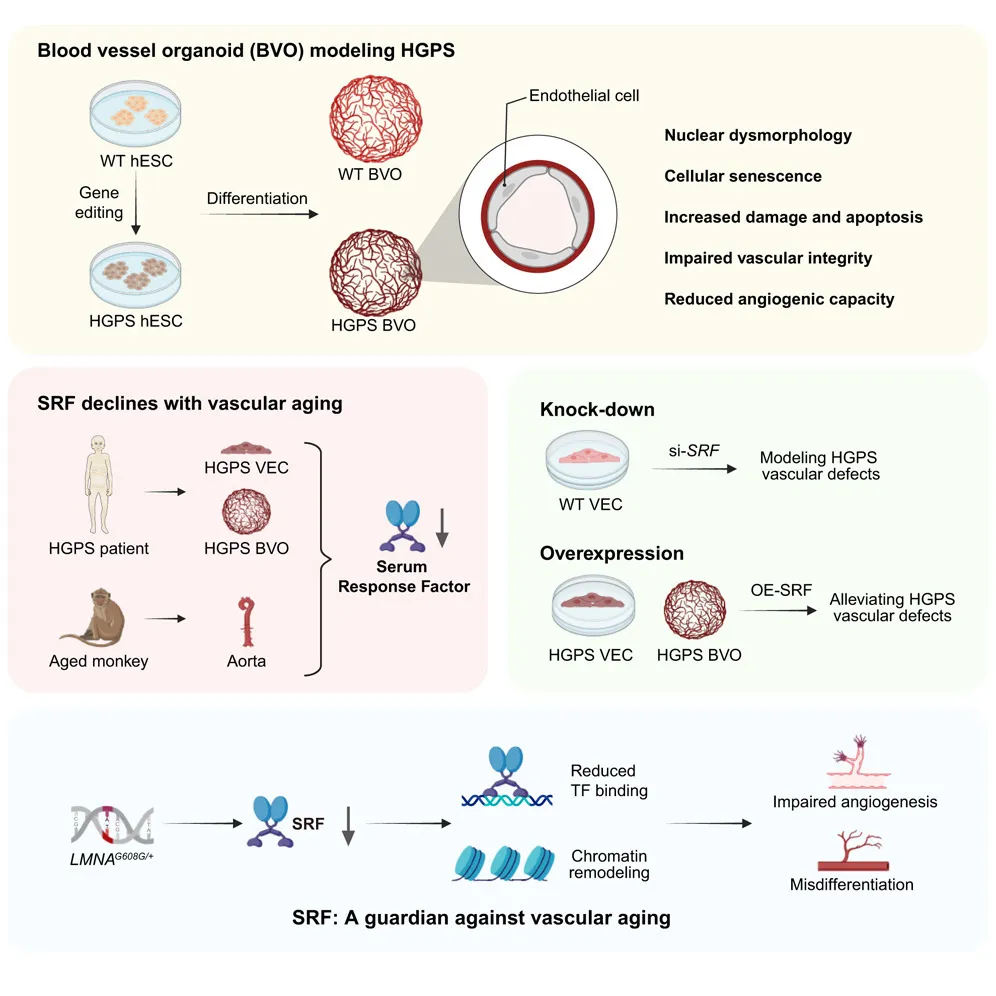
该研究利用基因编辑和人多能干细胞定向分化技术,首次成功构建了模拟 HGPS 的人类血管类器官模型。该模型在三维尺度上高度重现了 HGPS 患者血管系统的多种病理特征,包括早衰蛋白积累、核膜内陷、基底膜结构不连续以及血管屏障功能受损。此外,模型还表现出血管新生能力衰退、DNA 损伤增加、细胞凋亡增多及线粒体功能异常。
通过多维组学整合分析,研究人员发现,HGPS 血管类器官中下调的基因富集于血管发育和生成通路,并锁定转录因子 SRF 为核心调控因子。在 HGPS 模型及自然衰老的非人灵长类组织中,SRF 表达均显著下调,表明其下降是跨物种保守的血管衰老标志。功能实验证实,敲低 SRF 可重现血管衰老表型,而过表达 SRF 则能改善细胞核形态、减少 DNA 损伤并恢复血管生成能力。机制上,SRF 通过直接结合并维持下游促血管生成基因(如 VEGFA-VEGFR2 通路组分)的染色质开放性,驱动血管稳态维持。该研究确立了 SRF 在血管衰老中的关键作用,为防治心血管疾病提供了潜在靶点。
神经类器官模型揭示 YAP 缺失驱动人类神经管发育异常
神经发育障碍影响全球约 15% 的儿童和青少年,常导致认知、社交与运动功能受损。神经管缺陷(如无脑畸形)等疾病可追溯至胚胎早期神经管闭合过程的异常,该过程高度依赖机械力的精确调控,但机械信号如何与生化信号协同作用尚不明确。
近日,刘光慧研究员与首都医科大学宣武医院王思研究员合作,在 Science China Life Sciences 期刊发表了题为:Mechanosensor YAP Orchestrates Human Neural Rosette Morphogenesis via TEAD4–LEF1 Transcriptional Nexus 的研究论文。

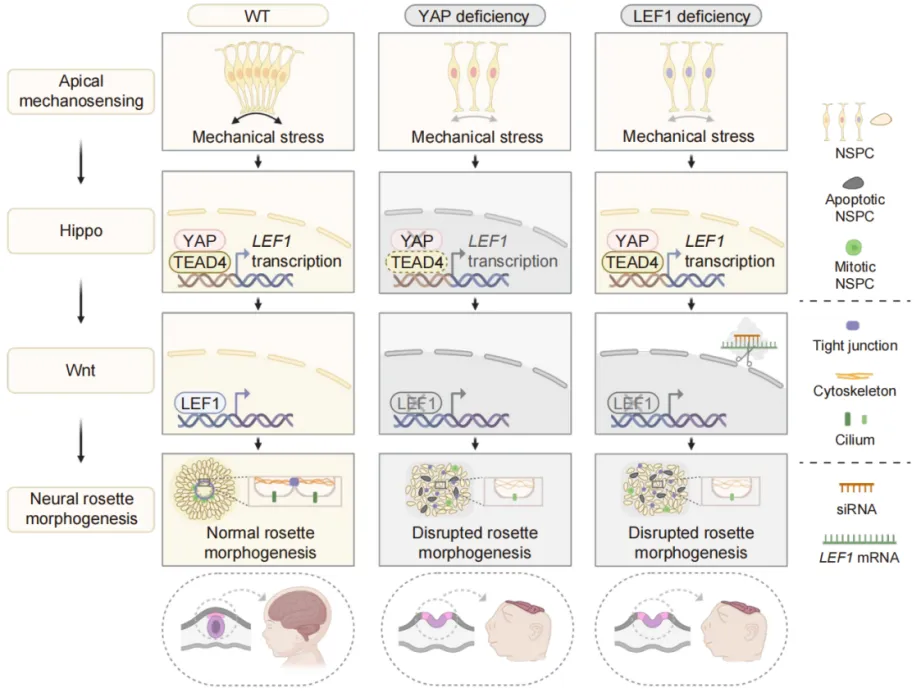
该研究利用人皮质类器官模型,揭示了 Hippo 通路核心效应因子 YAP 作为机械传感器在神经管形态发生中的核心作用。
该研究发现,YAP 在早期神经花环结构的高张力顶端区域富集并发生核转位,响应力学微环境。通过 CRISPR-Cas9 技术构建 YAP 敲除的人胚胎干细胞模型,研究团队发现 YAP 缺失导致神经干/祖细胞顶端-基底极性破坏,表现为细胞骨架紊乱、紧密连接蛋白分布异常和纤毛发生受损,最终阻碍神经花环形成。整合单细胞核 RNA 测序与染色质可及性测序数据,揭示 YAP 缺失后 Wnt 通路核心转录因子 LEF1 表达显著下调。进一步实验表明,YAP 与 TEAD4 形成转录复合体,直接结合 LEF1 启动子并激活其转录。功能回复实验证实,LEF1 过表达可部分挽救YAP缺失引起的结构异常。
该研究首次提出了“YAP–TEAD4–LEF1”调控轴线在神经管发育中的关键角色,阐明了机械力信号通过 Hippo 与 Wnt 通路交叉对话调控神经发育的机制,为神经管缺陷的干预提供了新理论基础。
展望
研究团队通过构建血管和神经类器官模型,分别从衰老和发育角度揭示了器官稳态调控的分子机制。血管类器官研究确立了 SRF 作为延缓血管衰老的潜在靶点,而神经类器官工作则阐明了 YAP 在机械力调控发育中的核心作用。这些成果不仅展示了类器官模型在模拟人类生理和病理过程中的优势,也为理解器官发育、维持和衰老的共性规律提供了新视角,未来有望推动相关疾病的早期诊断和靶向治疗策略开发。
论文链接:
https://www.cell.com/developmental-cell/abstract/S1534-5807(25)00690-2
https://www.sciengine.com/SCLS/doi/10.1007/s11427-025-3130-4
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


